- +7 (495) 74-88-777
- info@mda-cro.com
- 121096, г. Москва Краснопресненская наб., д. 12, подъезд №3, офис 1104а
- Пон - Чт: 9:00 - 18:00, Пт: 8:00 - 16:00
Минздрав России добавит возможность внесения новых данных по безопасности лекарственных средств без проведения экспертизы в досье зарегистрированных препаратов. Обновление регдосье будет возможно при условии, что новые данные по безопасности будут вноситься на основании информации экспертного учреждения – ФГБУ «НЦЭСМП» Минздрава РФ, – размещенного на сайте ведомства. В настоящее время допускается внесение изменений без экспертизы только в случае юридических изменений производителя,…
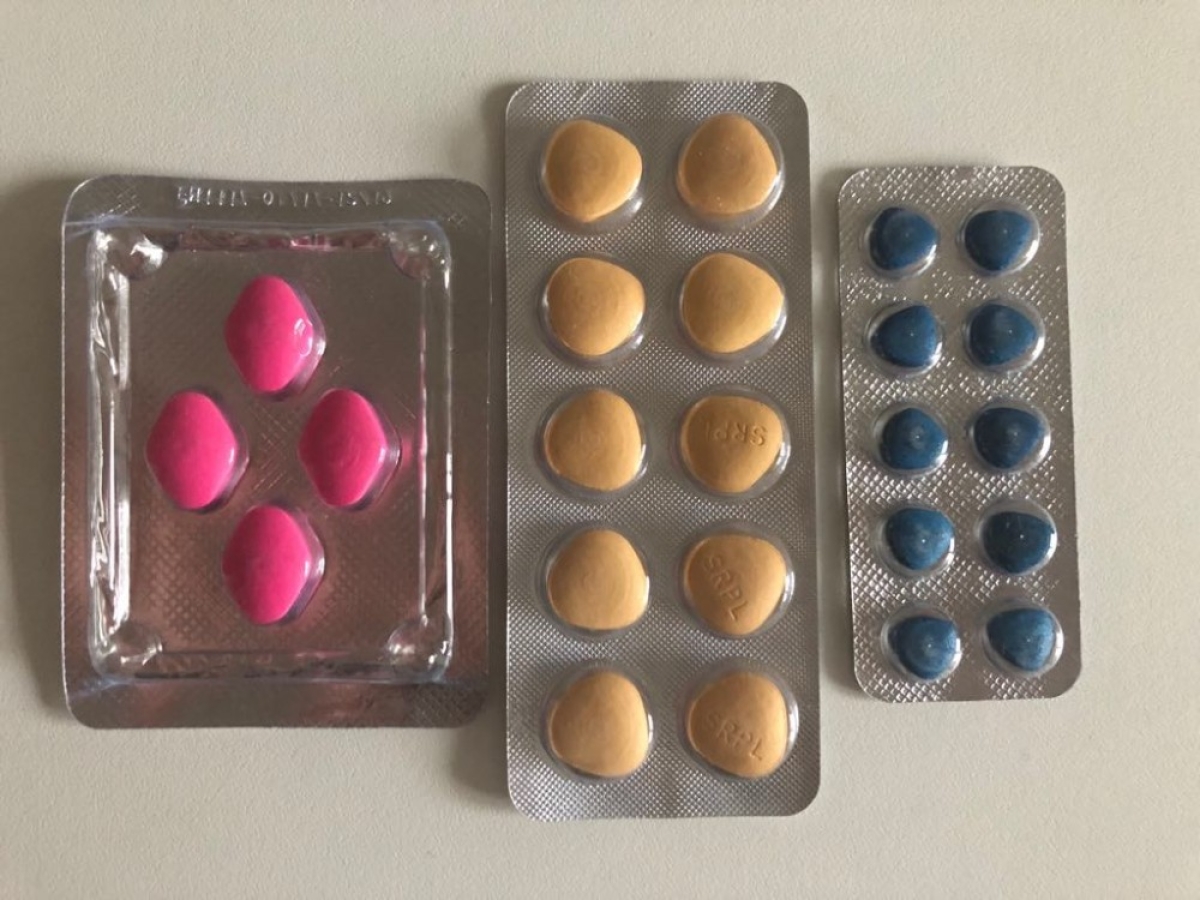
Депутаты Госдумы предложили поправки в Гражданский кодекс, которые позволят ускорить процедуру вывода дженериков на рынок после окончания патентной защиты оригинальных препаратов. Законопроект подлежит применению к правоотношениям, возникшим с 24 февраля 2022 года. Документ есть в распоряжении «ФВ». Депутаты от фракции «Справедливая Россия — патриоты — за правду» внесли в Государственную думу законопроект, дополняющий статью 1359 части 4 Гражданского кодекса новым…
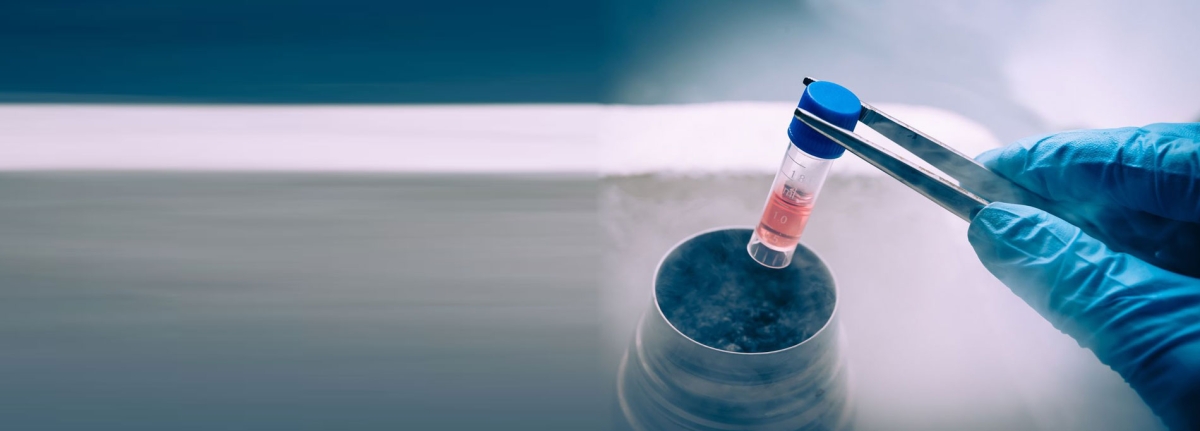
Правительство опубликовало два постановления, касающиеся биомедицинских клеточных продуктов. Первый документ устанавливает порядок обращения БМКП, а второй регулирует правила предоставления, подтверждения и отмены разрешения на производство и применение. Правительство утвердило порядок обращения биомедицинских клеточных продуктов (БМКП) для индивидуального применения. Соответствующее постановление № 384 от 28.03.2024 вступит в силу с 1 сентября 2024 года и будет действовать до 1 сентября 2030 года.…
Последние новости
-
 АПФ просит Минпромторг упростить для производителей из РФ подачу документов на регистрацию ЛП
АПФ просит Минпромторг упростить для производителей из РФ подачу документов на регистрацию ЛП
-
 Совет ЕЭК изменил правила проведения исследований биоэквивалентности лекарств
Совет ЕЭК изменил правила проведения исследований биоэквивалентности лекарств
-
 Совет ЕЭК принял Правила проведения инспекций системы фармаконадзора ЕАЭС
Совет ЕЭК принял Правила проведения инспекций системы фармаконадзора ЕАЭС
-
 Регулятор расширит перечень вносимых в регдосье лекарств изменений без проведения экспертизы
Регулятор расширит перечень вносимых в регдосье лекарств изменений без проведения экспертизы
-
 Депутаты внесли в Госдуму законопроект по ускорению вывода дженериков на рынок
Депутаты внесли в Госдуму законопроект по ускорению вывода дженериков на рынок